Liên kết cộng hóa trị là một trong những liên kết hóa học cơ bản. Liên kết này sẽ giải thích được sự hình thành các phân tử trong hóa học. Vậy, như thế nào là một LK cộng hóa trị, có mấy loại liên kết và cấu trúc của nó ra sao? Chúng ta sẽ cũng tìm hiểu rõ về các khái niệm này trong bài viết hôm nay nhé!
I. Liên kết cộng hóa trị là gì?
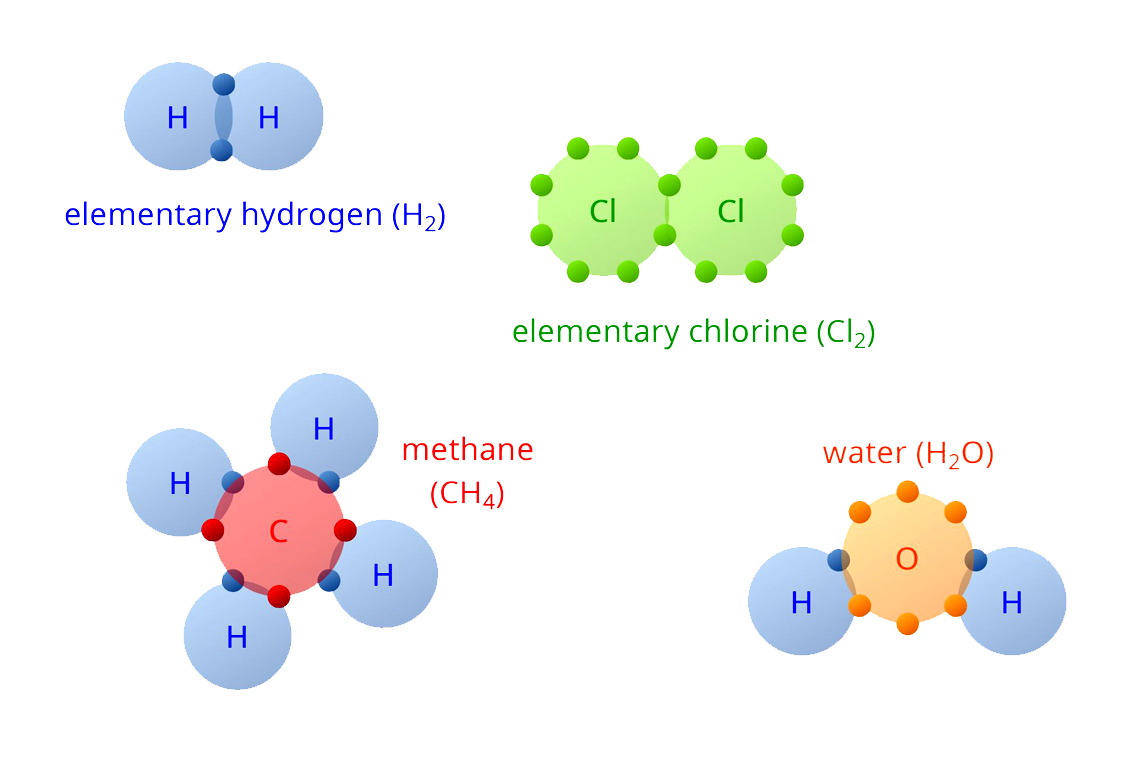
Liên kết cộng hóa trị (Covalent bond) là một loại liên kết hóa học được hình thành bằng việc dùng chung một hay nhiều cặp electron giữa các nguyên tử. Những cặp e này được gọi là cặp electron dùng chung. Việc dùng chung các electron này giúp các nguyên tử trong phân tử đạt được cấu hình electron bền vững.
Thuật ngữ liên kết cộng hóa trị (tiếng anh là covalent bond) được sử dụng vào năm 1939 với tiền tố co- có nghĩa là cùng nhau.
Loại liên kết này không chỉ hình thành với các nguyên tử cùng loại mà còn với các nguyên tử khác nhau.
II. Phân loại liên kết cộng hóa trị
Liên kết cộng hóa trị có liên quan đến các obitan nguyên tử. Các obitan (trừ obitan s) có định hướng trong không gian đặc biệt dẫn đến hình thành các loại liên kết khác nhau.
Liên kết cộng hóa trị mạnh mẽ nhất là liên kết sigma (σ) hình thành do sự chồng chéo obitan của hai nguyên tử. Liên kết sigma (σ) thường là liên kết đơn. Liên kết pi (π) yếu hơn do sự chồng chéo của các obitan p (hoặc obitan d). Liên kết đôi giữa hai nguyên tử gồm một liên kết sigma (σ) và một liên kết pi (π). Liên kết ba gồm một liên kết sigma (σ) và hai liên kết pi (π).
Người ta phân loại liên kết cộng hóa trị thành LK CHT có cực và LK CHT không cực. Liên kết này bị ảnh hưởng bởi độ âm điện của các nguyên tử trong liên kết. Liên kết giữa hai nguyên tử có độ âm điện tương đương là liên kết không phân cực. Người ta có thể dựa vào giá trị hiệu độ âm điện để dự đoán loại liên kết của hai nguyên tử.
1. Liên kết cộng hóa trị không cực
Có hiệu độ âm điện nhỏ hơn 0.4, cặp electron dùng chung nằm giữa hai nguyên tử. Sự hình thành liên kết giữa hai nguyên tử của cùng một nguyên tố như H2, Cl2, O2… có hiệu độ âm điện bằng 0. Khi hai nguyên tử tham gia liên kết có hiệu độ âm điện < 0.4, độ phân cực nhỏ đến mức không thể xác định được trong thực tế nên vẫn được coi là liên kết không phân cực.
2. Liên kết cộng hóa trị có cực
Có hiệu độ âm điện có giá trị từ 0.4 đến nhỏ hơn 1.7. Trong liên kết này, cặp electron dùng chung bị lệch về một phía. Ví dụ: liên kết O-H có hiệu độ âm điện bằng 1.24, liên kết H-Cl là 0.96…
Trường hợp hiệu độ âm điện từ 1.7 trở lên thì liên kết đó là liên kết ion.
3. Liên kết cho nhận
Trong một số trường hợp, cặp electron dùng chung chỉ do 1 nguyên tử đóng góp thì liên kết đó được gọi là liên kết cho nhận. Ví dụ như phân tử SO2.
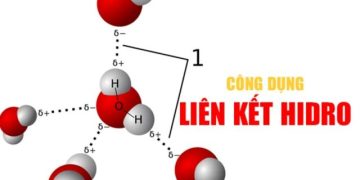
4. Liên kết hidro
Liên kết hidro thực tế là một liên kết cộng hóa trị, được hình thành từ lực hút tĩnh điện chủ yếu giữa nguyên tử Hidro (H) liên kết cộng hóa trị với một nguyên tử hoặc nhóm nguyên tử có độ âm điện cao hơn.
III. Sự lai hóa các obitan nguyên tử
Lai hóa obitan là sự tổ hợp các obitan hóa trị của một nguyên tử ở những phân lớp khác nhau tạo thành các orbital lai hóa giống nhau để xen phủ với các obitan hóa trị của các nguyên tử khác, tạo thành liên kết CHT. Các kiểu lai hóa thường gặp là sp, sp2, sp3.
IV. Tính chất của liên kết cộng hóa trị
Các chất trong phân tử chỉ có liên kết CHT có thể là:
- chất rắn: đường, iot, lưu huỳnh…
- chất lỏng: ancol, nước…
- chất khí: hidro, clo, oxi, cacbonic…
Các chất có cực và không cực thì:
- có cực: rượu etylic, đường tan nhiều trong dung môi phân cực
- không cực: iot, các chất hữu cơ không cực tan nhiều trong dung môi không phân cực như benzen, cacbon tetraclorua…
Nhìn chúng, các chất có lk CHT không cực không dẫn điện dù ở trạng thái nào đi nữa.
V. So sánh liên kết cộng hóa trị và liên kết ion
– Giống nhau: về nguyên nhân hình thành liên kết. Các nguyên tử liên kết với nhau tạo thành phân tử để đạt cấu hình bền của khí hiếm.
– Khác nhau:
- Về bản chất liên kết: Liên kết ion có bản chất là lực hút tĩnh điện giữa các ion mang điện tích trái dấu. Trong khi đó, bản chất của lk cộng hóa trị là sự dùng chung các electron.
- Về điều kiện xảy ra: liên kết ion chỉ xảy ra giữa những nguyên tố khác nhau (thường là kim loại điển hình liên kết với phi kim điển hình). Trong lk cộng hóa trị, liên kết xảy ra giữa các nguyên tố giống nhau hoặc gần giống nhau về bản chất hóa học (thường xảy ra với các nguyên tố nhóm IVA, VA, VIA, VIIA).
Trong thực tế, hầu hết các trường hợp trạng thái liên kết vừa mang tính chất của liên kết ion và liên kết cộng hóa trị. Do đó, người ta có thể dựa vào giá trị hiệu độ âm điện để xem loại liên kết nào chiếm ưu thế hơn.
Lời kết
Vậy là chúng ta đã cùng nhau tìm hiểu liên kết cộng hóa trị là gì, nó được phân loại như thế nào rồi phải không ạ. Bên cạnh đó, chúng ta cũng biết được mối liên hệ giữa hiệu độ âm điện và sự phân cực của liên kết. Ngoài ra, chúng ta cũng đã hiểu về liên kết đơn, liên kết đôi và liên kết ba được hình thành như thế nào. Ngoài ra, các bạn có thể tìm hiểu thêm về liên kết kim loại để xem bản chất của chúng có gì giống và khác lk cộng hóa trị nhé! Hi vọng bài viết này hữu ích với các bạn! Chúc các bạn thành công nhé!