Phản ứng phân hủy là gì? Tìm hiểu khái niệm, đặc điểm, phân loại, ví dụ minh họa và ứng dụng thực tiễn của phản ứng phân hủy trong học tập và đời sống hàng ngày.
Trong môn Hóa học, có nhiều loại phản ứng khác nhau giúp chúng ta hiểu cách các chất biến đổi. Một trong số đó là phản ứng phân hủy – khi một chất bị tách thành hai hay nhiều chất mới. Loại phản ứng này không chỉ xuất hiện trong sách vở mà còn có mặt trong nhiều hiện tượng quen thuộc hằng ngày. Vậy phản ứng phân hủy là gì? Có những ví dụ và ứng dụng nào dễ nhớ? Hãy cùng khám phá nhé!
Phản ứng phân hủy là gì? (ảnh minh họa)
1. Phản ứng phân hủy là gì?
Phản ứng phân hủy là một loại phản ứng hóa học trong đó một chất bị phân tách thành hai hoặc nhiều chất đơn giản hơn. Phản ứng này thường xảy ra khi có tác động của nhiệt độ, ánh sáng hoặc dòng điện.
Công thức tổng quát:
A → B + C
(Trong đó A là chất ban đầu, B và C là các chất tạo thành)
Ví dụ đơn giản:
CaCO₃ → CaO + CO₂
(Đây là phản ứng phân hủy đá vôi thành vôi sống và khí CO₂ khi đun nóng.)
Phản ứng phân hủy giúp chúng ta hiểu rõ hơn về cấu tạo và tính chất của các chất. Đây là một phần kiến thức quan trọng trong chương trình hóa học lớp 8 và rất dễ gặp trong thực tế.
2. Đặc điểm của phản ứng phân hủy
Phản ứng phân hủy có một số đặc điểm dễ nhận biết như sau:
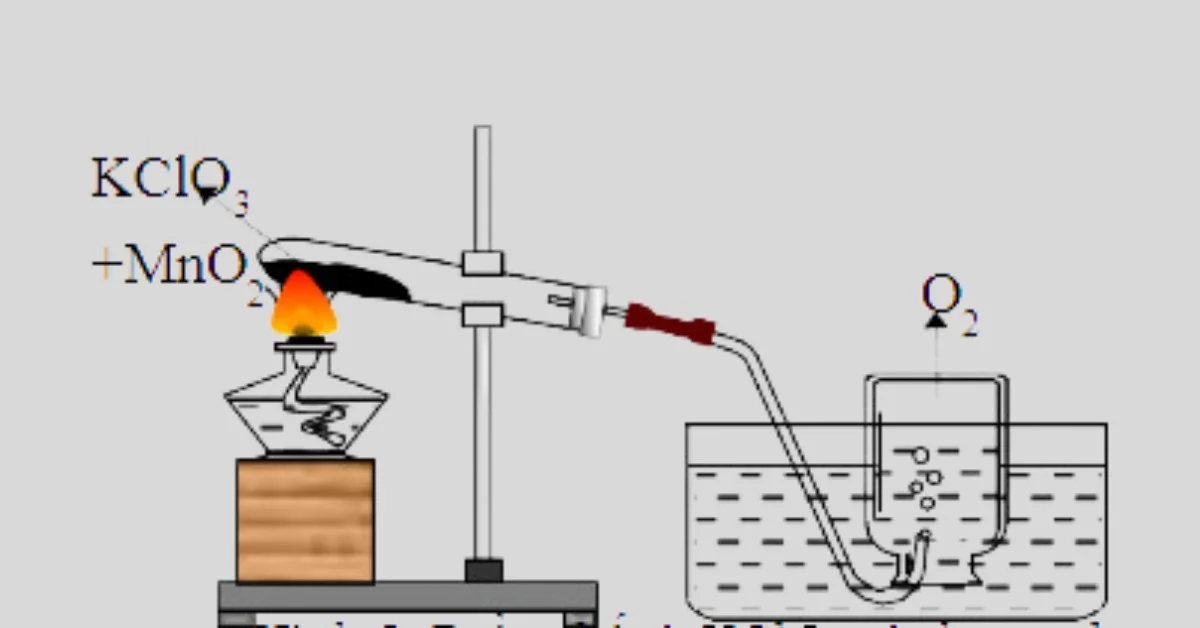
Phản ứng phân hủy KClO₃
✅ Một chất tạo thành hai hoặc nhiều chất mới: Sản phẩm sau phản ứng thường là các chất đơn giản hơn so với chất ban đầu.
✅ Thường cần có điều kiện tác động: Nhiệt độ cao, ánh sáng hoặc dòng điện thường được dùng để phản ứng xảy ra.
✅ Có thể sinh ra khí hoặc chất rắn mới: Nhiều phản ứng phân hủy tạo ra khí (như O₂, CO₂) hoặc chất rắn (như kim loại, oxit).
✅ Thường gặp ở các chất không bền: Một số hợp chất dễ bị phân hủy nếu bị nung nóng hoặc chiếu sáng.
🔎 Ví dụ minh họa:
2HgO → 2Hg + O₂
(Khi nung thủy ngân oxit, ta thu được thủy ngân và khí oxi.)
Những đặc điểm trên sẽ giúp bạn dễ dàng nhận biết và phân biệt phản ứng phân hủy với các loại phản ứng hóa học khác.
3. Phân loại phản ứng phân hủy
Phản ứng phân hủy được chia thành nhiều loại dựa trên điều kiện xảy ra phản ứng hoặc loại chất bị phân hủy. Cụ thể như sau:
a) Theo điều kiện tác động
Phản ứng nhiệt phân
👉 Là phản ứng xảy ra khi đun nóng chất.
Ví dụ: CaCO₃ → CaO + CO₂
(Đá vôi phân hủy khi nung nóng.)
Phản ứng quang phân
👉 Là phản ứng xảy ra khi có ánh sáng chiếu vào.
Ví dụ: 2AgCl → 2Ag + Cl₂ (dưới ánh sáng)
(Chất nhạy sáng phân hủy thành bạc kim loại và khí clo.)
Phản ứng điện phân
👉 Là phản ứng xảy ra khi dòng điện chạy qua dung dịch hoặc chất lỏng nóng chảy.
Ví dụ: 2H₂O → 2H₂ + O₂ (dưới tác dụng dòng điện)
(Phân hủy nước thành khí hydro và oxy.)
b) Theo chất ban đầu
Phân hủy chất vô cơ:
Bao gồm oxit, bazơ, muối, axit…
Ví dụ: 2KClO₃ → 2KCl + 3O₂
Phân hủy chất hữu cơ:
Như rượu, đường, hydrocacbon… thường xảy ra trong quá trình đốt cháy hoặc phân hủy nhiệt.
Ví dụ: C₂H₅OH → C₂H₄ + H₂O (khi có nhiệt và xúc tác)
4. Vai trò và ứng dụng của phản ứng phân hủy
Phản ứng phân hủy không chỉ là kiến thức quan trọng trong sách giáo khoa mà còn có nhiều ứng dụng thiết thực trong đời sống và công nghiệp. Dưới đây là một số vai trò tiêu biểu:
✅ Trong đời sống hằng ngày
Sản xuất vôi sống (CaO) từ đá vôi (CaCO₃):
Ứng dụng trong xây dựng, xử lý môi trường, khử chua đất nông nghiệp.
Điện phân nước tạo khí oxy và hydro:
Khí hydro dùng làm nhiên liệu sạch, khí oxy cần cho y tế và công nghiệp.
Xử lý rác thải hữu cơ bằng phân hủy sinh học:
Giúp bảo vệ môi trường, tái chế chất hữu cơ thành phân bón.
✅ Trong công nghiệp
Chế tạo kim loại từ quặng bằng cách phân hủy hợp chất chứa kim loại.
Ví dụ: Nung Fe₂O₃ trong luyện kim để thu được sắt.
Chế tạo khí công nghiệp:
Ví dụ: O₂ thu từ nhiệt phân KClO₃, dùng trong hàn cắt kim loại.
Ứng dụng trong phản ứng dây chuyền:
Một số phản ứng phân hủy tạo sản phẩm trung gian dùng cho phản ứng khác trong dây chuyền sản xuất.
✅ Trong y học và nghiên cứu
Phân tích thành phần chất bằng cách phân hủy để tìm ra cấu tạo.
Tạo khí vô trùng như O₂ cho phòng mổ, cứu hộ khẩn cấp.
5. Một số ví dụ minh họa về phản ứng phân hủy
Dưới đây là bảng tổng hợp các ví dụ phổ biến của phản ứng phân hủy theo từng loại:
| Loại phản ứng phân hủy | Phương trình hóa học | Ghi chú / Ứng dụng |
|---|---|---|
| Nhiệt phân | CaCO₃ → CaO + CO₂ | Sản xuất vôi sống trong xây dựng |
| 2HgO → 2Hg + O₂ | Thí nghiệm trong phòng học | |
| 2KClO₃ → 2KCl + 3O₂ | Điều chế khí oxi trong phòng thí nghiệm | |
| Quang phân | 2AgCl → 2Ag + Cl₂ (dưới ánh sáng) | Chất nhạy sáng, ứng dụng trong phim ảnh |
| Điện phân | 2H₂O → 2H₂ + O₂ (dòng điện) | Điều chế hydro và oxy tinh khiết |
| NaCl (lỏng) → Na + Cl₂ (dòng điện) | Điều chế kim loại và khí clo trong công nghiệp | |
| Phân hủy chất hữu cơ | C₂H₅OH → C₂H₄ + H₂O (nhiệt, xúc tác) | Phản ứng khử nước trong hóa hữu cơ |
6. Bài tập vận dụng và lời giải tham khảo
Để hiểu rõ hơn về phản ứng phân hủy, chúng ta cùng làm một số bài tập đơn giản và tham khảo lời giải dưới đây.
Bài tập 1: Phản ứng nhiệt phân
Câu hỏi: Viết phương trình phản ứng phân hủy của CaCO₃ khi nung nóng.
Lời giải:
Khi nung nóng, CaCO₃ phân hủy thành CaO và CO₂. Phương trình phản ứng như sau:
CaCO₃ -> CaO + CO₂↑
Giải thích:
CaCO₃: canxi cacbonat (có trong đá vôi)
CaO: canxi oxit (vôi sống)
CO₂: khí cacbonic (thoát ra ngoài môi trường)
Phản ứng này là một ví dụ điển hình của phản ứng phân hủy tỏa nhiệt, thường gặp trong sản xuất vôi sống.
Bài tập 2: Phản ứng quang phân
Câu hỏi: Phản ứng phân hủy nào xảy ra dưới tác dụng của ánh sáng?
Lời giải:
Phản ứng phân hủy xảy ra dưới tác dụng của ánh sáng được gọi là phản ứng phân hủy quang hóa (phản ứng quang phân). Một ví dụ điển hình là sự phân hủy của bạc clorua (AgCl) khi gặp ánh sáng:
2AgCl –(ánh sáng)-> 2Ag+Cl₂↑
Giải thích:
AgCl: bạc clorua – là một chất rắn màu trắng.
Dưới tác dụng của ánh sáng mặt trời, AgCl bị phân hủy tạo thành:
Ag: bạc – có màu xám (hoặc đen do bị ôxi hóa)
Cl₂: khí clo thoát ra.
Phản ứng này rất quan trọng trong công nghệ nhiếp ảnh và chế tạo các sản phẩm nhạy sáng.
Bài tập 3: Phản ứng điện phân
Câu hỏi: Viết phương trình phản ứng điện phân nước để tạo ra khí hydro và oxy.
Lời giải:
Khi điện phân nước, dưới tác dụng của dòng điện một chiều, nước (H₂O) bị phân hủy thành khí hidro (H₂) và khí oxi (O₂). Phương trình phản ứng tổng quát như sau:
2H₂O –(điện phân)->
Giải thích:
2H₂O: 2 phân tử nước
2H₂: khí hidro (thoát ra ở cực âm – catot)
O₂: khí oxi (thoát ra ở cực dương – anot)
Điện phân nước được sử dụng để tạo ra khí hydro cho các ứng dụng năng lượng.
Bài tập 4: Nhận diện phản ứng phân hủy
Câu hỏi: Dựa vào phương trình hóa học dưới đây, hãy cho biết đây là phản ứng phân hủy loại nào và viết tên của chất bị phân hủy.
2KClO₃ –(nhiệt độ)-> 2KCl+3O₂↑
Lời giải:
Phản ứng trên là phản ứng nhiệt phân của KClO₃ (kali clorat). Khi bị nung nóng, KClO₃ phân hủy thành KCl và O₂. Đây là một ví dụ điển hình về phản ứng phân hủy chất vô cơ.
7. Lời kết
Phản ứng phân hủy là một phần quan trọng trong hóa học, giúp chúng ta hiểu về quá trình biến đổi chất dưới tác động của nhiệt, ánh sáng, hoặc dòng điện. Qua các ví dụ và bài tập, bạn sẽ dễ dàng nhận biết các loại phản ứng phân hủy và ứng dụng chúng trong thực tế.
Hãy nhớ rằng, việc nắm vững đặc điểm, phân loại và ứng dụng của phản ứng phân hủy sẽ giúp bạn làm bài tập tốt hơn và áp dụng kiến thức vào các tình huống hằng ngày.